 更多“氨合成反应过程由气固相催化反应过程的()、()、()等一系列…”相关的问题
更多“氨合成反应过程由气固相催化反应过程的()、()、()等一系列…”相关的问题
第3题
某氮肥厂氨氮废水中的氮元素多以NH和NH3·H2O的形式存在,该废水的处理流程如下:![]()
问题一、过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。
①用离子方程式表示加NaOH溶液的作用:()。
②用化学平衡原理解释通空气的目的:()。
问题二、过程Ⅱ:在微生物作用的条件下,NH经过两步反应被氧化成NO。两步反应的能量变化示意图如下:
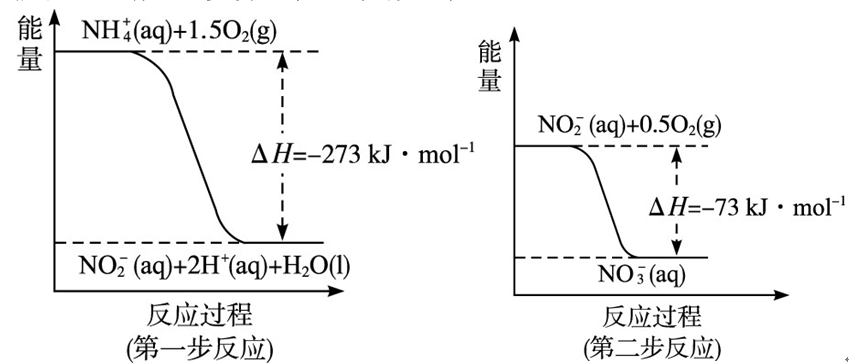
①第一步反应是()反应(选填“放热”或“吸热”),判断依据是()。
②1molNH(aq)全部氧化成NO(aq)的热化学方程式是()。
问题三、过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3复原成N2。假设该反应消耗32gCH3OH转移6mol电子,则参加反应的复原剂和氧化剂的物质的量之比是()。
第5题
在厌氧消化池中,下列有关影响因素C/N比的说法正确的是()。
A.碳源担负着双重任务,一是作为反应过程的能源,其二是合成新细胞
B.C/N比达到30∶1比较合适
C.C/N太高,细胞的氮量不足,消化液的缓冲能力高,pH值容易降低
D.C/N太低,氮量过多,pH值可能下降,铵盐容易积累,会抑制消化进程
第9题
化工生产的条件和环境较为苛刻,不同的生产工艺对于压力、温度的要求不尽相同。下列关于工艺的生产要求,说法错误的是()。
A.石油烃类裂解,裂解炉出口的温度高达950℃
B.石油烃类裂解而裂解产物气的分离需要在-50℃下进行
C.氨的合成要在10~30MP
D.300℃左右的条件下进行
E.乙烯聚合生产聚乙烯是在压力为130~300MP
F.温度为150~300℃的条件下进行


 如果结果不匹配,请
如果结果不匹配,请 
















