 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
实验室用如图装置模拟炼铁。下列说法正确的是()
A.该反应属于置换反应
B.应先加热Fe2O3,再通入CO
C.红棕色的Fe2O3粉末逐渐变黑
D.气体通过澄清石灰水后直接排放
 答案
答案
C、红棕色的Fe2O3粉末逐渐变黑
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.该反应属于置换反应
B.应先加热Fe2O3,再通入CO
C.红棕色的Fe2O3粉末逐渐变黑
D.气体通过澄清石灰水后直接排放
 答案
答案
C、红棕色的Fe2O3粉末逐渐变黑
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“实验室用如图装置模拟炼铁。下列说法正确的是()”相关的问题
更多“实验室用如图装置模拟炼铁。下列说法正确的是()”相关的问题
A.磁铁矿的主要成分是Fe2O3
B.应先加热Fe2O3,再通入CO
C.红棕色的Fe2O3逐渐变黑
D.气体通过澄清石灰水后可直接排放
A.该实验进行时需要先加热Fe2O3再通入CO
B.C可以用点燃的方法对尾气进行处理
C.D在A处CO发生了还原反应
A.稀释浓硫酸时,先在烧杯内倒入水,再缓慢注入浓硫酸,并不断搅拌
B.用托盘天平称量药品时,先调节天平平衡,再称量
C.实验室用CO与Fe2O3反应制取铁时,先通CO,再点燃酒精灯
D.实验室制取气体时,先装药品,再检查装置气密性
如图为实验室模拟还原氧化铁的实验装置(夹持仪器等省略),已知: 。下列说法合理的是()。
。下列说法合理的是()。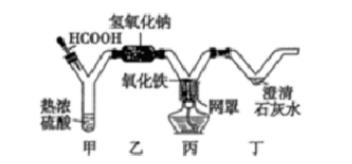
A.
装置丙中发生反应的化学方程式为:
B.装置乙中氢氧化钠的作用是吸收、除去二氧化碳
C.与课本模拟工业炼铁装置相比,该装置环保无污染
D.装置丁处装入澄清石灰水的目的是检验生成的CO2
A.实验室用CO还原氧化铁时,先通一会CO,再加热,所以实验结束后,也先停止通气体
B.碳酸盐与盐酸反应放出气体,则与盐酸反应放出气体的物质一定是碳酸盐
C.碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性
D.化合物都是由不同种元素组成的,所以不同种元素组成的物质一定是化合物
A.实验室用加热高锰酸钾制取氧气:2KMnO4eq \o(=====,\s\up7(△))K2MnO4+MnO2+O2↑,分解反应
B.铁丝在氧气中燃烧:4Fe+3O2eq \o(=====,\s\up7(点燃))2Fe2O3,化合反应
C.高炉炼铁原理:Fe2O3+3COeq \o(=====,\s\up7(高温))2Fe+3CO2,复分解反应
D.将铁片投入足量的稀盐酸中:2Fe+6HCl===2FeCl3+3H2↑,置换反应
侯氏制碱法制备碳酸氢钠的原理为NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓,某化学小组用如图装置在实验室中模拟该制备过程,下列说法不正确的是()。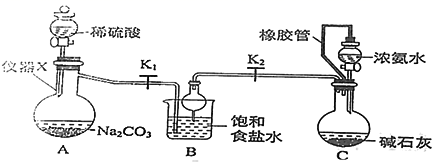
A.装置A中仪器X的名称为蒸馏烧瓶
B.装置B中球形干燥管的作用是防止倒吸
C.装置C中橡胶管的作用是平衡压强,使溶液顺利滴下
D.实验开始后,应先打开K1一段时间,然后再打开K2
实验室里可用甲醇等有关物质制备HCHO,关于甲醇和甲醛的沸点和水溶性见下表: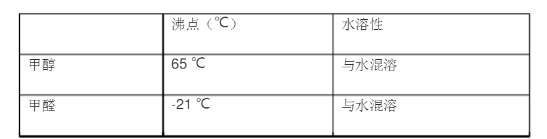 某校化学兴趣小组的甲、乙两位同学,在研究性学习中,运用以上信息和已有知识分别设计了二套实验室制取HCHO装置,如图甲和乙。
某校化学兴趣小组的甲、乙两位同学,在研究性学习中,运用以上信息和已有知识分别设计了二套实验室制取HCHO装置,如图甲和乙。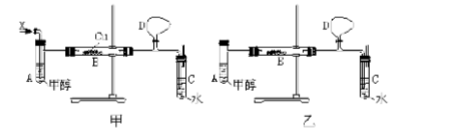
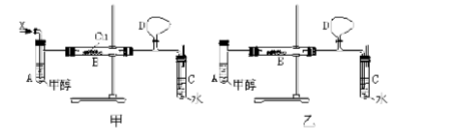 据此请你回答下列问题:
据此请你回答下列问题:
(1)若按甲装置进行实验,则通入A试管的X应是();B中反应的化学方程式是()。
(2)若按乙装置进行实验,则B管中应装入()。
(3)当实验完成时,若在C中滴加适量银氨溶液,并用水浴将C加热,发生反应的化学方程式是()。
(4)在反应过程中,甲、乙两种装置中都需直接加热的仪器是()(填A、B、C)。
(5)实验开始时,先打开气球D的开关,直至实验结束。气球D的作用是()。
(6)从生成甲醛的产量来看,你认为两套装置中较好的是()(填“甲”或“乙”)。
A.用铁跟稀盐酸反应制取氯化铁:2Fe + 6HCl = 2FeCl3 + 3H2↑
B.用铜粉加热除去空气中的氧气:2Cu+ O2 加热 2CuO
C.用一氧化碳还原氧化铁炼铁: Fe2O3 + 3CO 高温2Fe + 3CO2
D.用含氢氧化铝的药物治疗胃酸过多症:Al(OH)3 + 3HCl = AlCl3 + 3H2O
A.给酒精灯加网罩,目的是使火焰集中并提高温度
B.实验过程中,可观察到红棕色粉末逐渐变黑
C.木炭是使氧化铜还原为铜的物质,它具有氧化性
D.实验结束后,应先停止加热,再将导气管从澄清石灰水中撤出