 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列离子在溶液中因发生氧化还原反应而不能大量共存的是()
A.H3O+、NO3-、Fe2+、Na+
B.g+、NO3-、Cl-、K+
C.K+、Ba2+、OH-、SO42-
D.u2+、NH4+、Br-、OH-
 答案
答案
A、H3O+、NO3-、Fe2+、Na+
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.H3O+、NO3-、Fe2+、Na+
B.g+、NO3-、Cl-、K+
C.K+、Ba2+、OH-、SO42-
D.u2+、NH4+、Br-、OH-
 答案
答案
A、H3O+、NO3-、Fe2+、Na+
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列离子在溶液中因发生氧化还原反应而不能大量共存的是()”相关的问题
更多“下列离子在溶液中因发生氧化还原反应而不能大量共存的是()”相关的问题
A.g+,Ca2+,Br-,S2-
B.H+,Na+,S2-,NO3-
C.H+,SO32-,Na+,CO32-
D.Na+,NO3-,HCO3-,OH-
A.21:5
B.11:3
C.5:1
D.3:1
A.仅被氧化
B.仅被还原
C.既被氧化又被还原
D.既未被氧化又未被还原
A.2个
B.3个
C.4个
D.5个
KMnO4是一种重要消毒剂,俗名叫灰锰氧。
Ⅰ.某工厂以废旧锌锰电池为原料制备高锰酸钾的流程如下(部分产物已省略)
回答下列问题: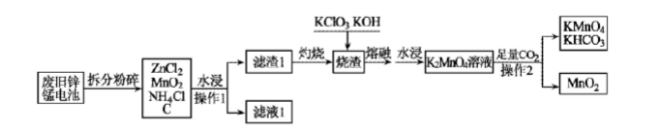 (1)K+的结构示意图为()。
(1)K+的结构示意图为()。
(2)这种锌锰电池放电时,负极的电极反应式为()。
(3)滤渣1“灼烧”的目的是();可循环利用的物质是()(填化学式)。
(4)“水浸”采用适当加热搅拌等措施,其目的是(),熔融“烧渣”可能产生的大气污染物是()。
(5)向K2MnO4溶液中通入足量CO2的离子方程式为:()。
Ⅱ.实验室中利用K2MnO4进行如下实验,下列说法错误的是()。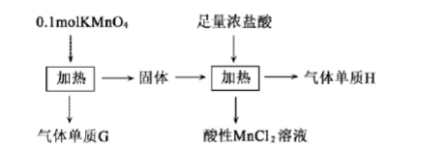 A、G与H均为氧化产物
A、G与H均为氧化产物
B、实验中KMnO4只作氧化剂
C、Mn元素至少参与了3个氧化还原反应
D、G与H的物质的量之和可能为0.25mol
A.在该反应中碘酸钠作还原剂
B.碱性条件下,氯气的氧化性强于高碘酸钠的氧化性
C.反应中氧化产物与还原产物的物质的量之比为2:1
D.反应中生成1molNa2H3IO6转移2mol电子
工业上用铝土矿(主要成分为氧化铝,含少量氧化铁)制取铝的过程如图所示: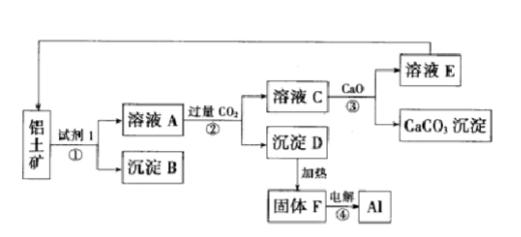 请回答:
请回答:
(1)试剂Ι为()(填化学式),①-④转化中属于氧化还原反应的是()(填序号);
(2)沉淀B的化学式为(),写出该物质发生铝热反应的化学方程式();
(3)电解F,当转移0.6mol,电子时,可制得铝()g;
(4)沉淀D是药物“胃舒平”的主要成分,可用于治疗胃酸(稀盐酸)过多,写出该反应的离子方程式();
(5)②中发生反应的离子方程式为()。
A.乙烯使溴的四氯化碳溶液褪色
B.将苯加入溴水中,振荡后水层接近无色
C.将苯、浓硫酸、浓硝酸混合后在50~60℃水浴中加热
D.液态植物油与氢气反应生成固态物质