 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[填空题]
反应N2O5→2NO2+1/2O2在298K时的速率常数为3.46×10-5s-1,在318K时的速率常数为4.98×10-4s-1,则308K时的反应速率常数为()10-4s-1。(保留两位小数)
暂无答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“反应N2O5→2NO2+1/2O2在298K时的速率常数为3…”相关的问题
更多“反应N2O5→2NO2+1/2O2在298K时的速率常数为3…”相关的问题
A.2Na2O2+2Mn2O7→4NaMnO4+O2↑
B.2Na2O2+P2O3→Na4P2O7
C.2Na2O2+2 N2O3→NaNO2+O2↑
D.2 Na2O2+2 N2O5 →4NaNO3+O2↑
A.v(N2O5)=1.8×10-4mol·L-1·s-1
B.v(N2O5)=1.8×10-2mol·L-1·s-1
C.v(NO2)=1.8×10-4mol·L-1·s-1
D.v(O2)=1.8×10-4mol·L-1·s-1
A.(1)属于化合反应
B.(2)(3)属于置换反应
C.(4)属于复分解反应
D.(2)属于置换反应
某化学小组的同学为探究原电池原理,设计如图所示装置,将锌、铜通过导线相连,置于稀硫酸中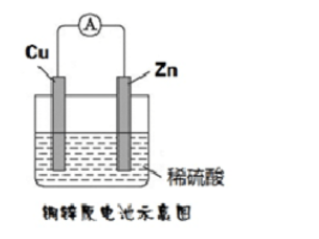 (1)外电路,电子从()极流出。溶液中,阳离子向()极移动。
(1)外电路,电子从()极流出。溶液中,阳离子向()极移动。
(2)若反应过程中有0.2mol电子发生转移,则生成的气体在标准状况下的体积为()。
(3)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是()(填序号)。
A.无水乙醇
B.醋酸溶液
C.CuSo4溶液
D.苯
(4)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是()(填字母代号)。
A.NaOH+HCl=NaCl+H2O
B.2H2+O2=2H2O
C.Fe+2FeCl3=3FeCl2
D.2H20=2H2↑+2O2↑
A.H2O2 ==== H2↑+ O2↑
B.H2O + CO2 === H2CO3
C.H2O ==== H2↑+ O2↑
D.3Fe + 2O2 === Fe3O4