 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将20 g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定质量的稀硫酸恰好完全反应,所得溶液质量为80.5 g,同时生成氢气 0.4 g,试计算: (1)样品中锌的质量为()g。 (2)完全反应后所得溶液中溶质的质量分数(写出计算过程)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“将20 g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定…”相关的问题
更多“将20 g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定…”相关的问题
十二水合硫酸铝钾[KAI(SO4)2・12H2O]俗名明矾,在生活、医药、工业上应用广泛。下面是实脸室探究从铝土矿(主要成分是氧化铝,含少量氧化铁和二氧化硅杂质)制备明矾的流程示意图。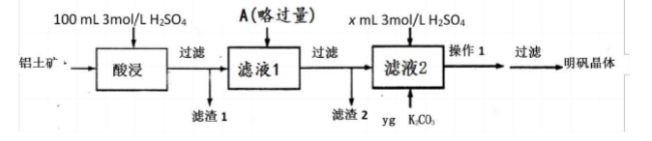 已知:二氧化硅不溶于水,也不与硫酸反应。
已知:二氧化硅不溶于水,也不与硫酸反应。
(1)铝元素在地壳中以()态存在,写出KAl(SO4)·12H2O溶于水的电离方程式()。当明矾溶液中混有NaCl时,简述如何检验Cl()。
(2)滤渣1主要为()(填化学式);以Al2O3为原料,制备该单质铝的反应方程式()。
(3)若A为金属单质,则滤渣2的成分有()。
(4)操作1是蒸发溶剂至有大量晶膜、冷却结晶。实验室进行该操作时,需要的实验仪器有铁架台、()。
(5)如图为某硫酸试剂瓶的标签。若用其配制100mL3mol/L的溶液,需该硫酸()mL(含ρ的表达式)。若此硫酸物质的量浓度为c1,35%的硫酸物质的浓度为c2,则c1()2c2(填大于,小于或等于)。 (6)工业生产中,获取明矾晶体后的母液应该()(填序号)。
(6)工业生产中,获取明矾晶体后的母液应该()(填序号)。
A、弃去
B、返回酸浸流程重复利用
C、返回滤液1重复利用
D、返回滤液2重复利用
A.厨房中的洗涤剂可以溶解餐具上的油污
B.N2,NO,NO2等含氮物质均为空气污染物
C.活性炭溶于水生成的胶状物可吸附杂质,达到净水目的
D.废旧电池的分类回收有利于保护环境
A.MgO、Al2O3的熔点很高,可制作耐高温材料
B.硫酸铝或硫酸铁溶于水,会生成氢氧化物胶体能吸附悬浮杂质,所以具有净水功能
C.l具有良好的延展性和抗腐蚀性,可制成铝箔包装物品
D.氧化铝不耐酸但是耐碱腐蚀,所以铝制容器不可盛放酸性物质,可盛放碱性物质
A.溶解废渣时不能用稀盐酸代替稀H2SO4
B.除去Cu2+可采用FeS
C.流程中a~b的目的是富集NiSO4
D.操作Ⅰ为蒸发浓缩、冷却结晶
A.纯度高(99.99%以上),杂质含量一般不得超过0.01%,个别的基准试剂杂质含量不超过0.02%,有已知灵敏度的定性方法可供检验其纯度
B.易获得、易精制、易干燥,使用时易溶于水(或稀酸、稀碱溶液);稳定性好,不易吸水,不吸收二氧化碳,不被空气氧化,干燥时不分解,便于精确称量和长期保存
C.使用中符合化学反应的要求,组成恒定,标定时能按化学反应式定量完成,没有副反应或逆反应等,便于计算
D.为减小称量的相对误差,所选用的基准试剂中,目标元素的质量应比较小,这样可增大其称量
A.温度和溶剂种类对NaOH的溶觯度都有影响
B.NaOH易溶于水,也易溶于酒精
C.40℃,40 gNaOH溶解在l00 g酒精中达到饱和
D.将等质量40℃的饱和NaOH水溶液和饱和NaOH酒精溶液降温至20C,析出的晶体前者比后者多
A.③①②⑤④
B.①⑤③②④
C.①③⑤④②
D.①③②⑤④
工业上利用铅浮渣(主要成分是PbO,Pb,含有少量Ag,CaO和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示: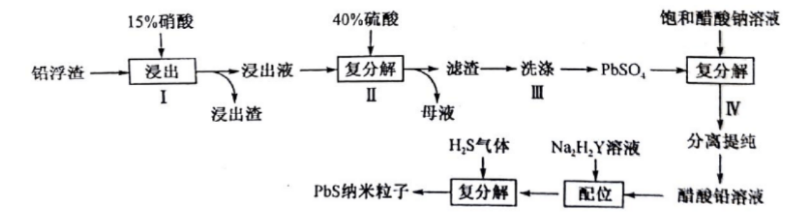 已知:25℃时,
已知:25℃时,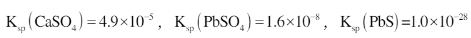 (1)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有()。
(1)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有()。
(2)写出Pb参加反应的化学方程式:()。保持铅剩余的原因是()。
(3)母液的主要成分是()(写化学式),可以循环利用。若母液中残留的SO42-过多,循环利用时可能出现的问题是()。
(4)若浸出液中c(Ca=2+)=0.05mol.L-1,步骤Ⅱ当pb2+完全沉淀后滤渣中是否有CaSO4存在?()(填有或没有)理由是()(通过计算说明)。