 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一个绝热刚性容器中发生一化学反应,使系统的温度从T1升高到T2,压力从P1升高到P2,则()。
A.QvO,W<0,AU<0
B.Q=O,W=0,AU=O
C.Q=QW<0,AU<0
D.QvO,W=0,AU
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.QvO,W<0,AU<0
B.Q=O,W=0,AU=O
C.Q=QW<0,AU<0
D.QvO,W=0,AU
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在一个绝热刚性容器中发生一化学反应,使系统的温度从T1升高到…”相关的问题
更多“在一个绝热刚性容器中发生一化学反应,使系统的温度从T1升高到…”相关的问题
最近科学家提出“绿色自由”设想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。“绿色自由”设想技术流程如下
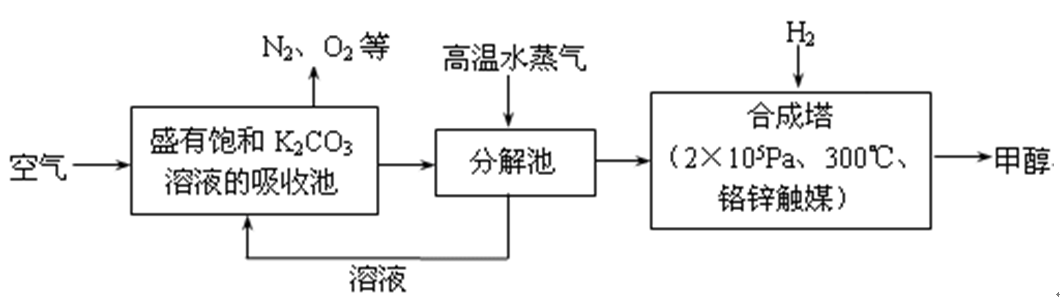
问题一、分解池中发生分解反应的物质是()。
问题二、在合成塔中,假设有CO2与足量H2kJ的热量,试写出合成塔中发生反应的热化学方程式()
问题三、①从平衡移动原理分析,低温有利于原料气的转化,而实际生产中采用300℃的温度,原因之一是考虑到催化剂的催化活性,原因之二是()。
②“绿色自由”设想技术流程中常包括物质和能量的“循环利用”,上述流程中能表达“循环利用”的除碳酸钾溶液外,还包括()。
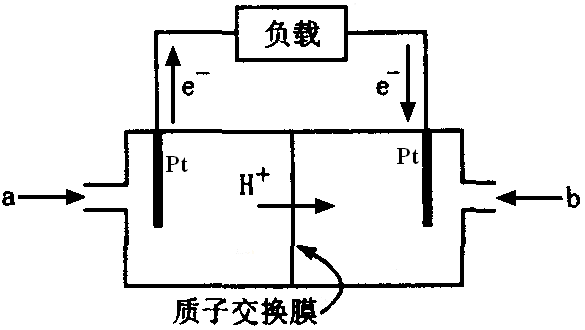
问题四、右图是甲醇燃料电池的结构示意图。已知电池总反应为:2CH3OH+3O2=2CO2+4H2O。通入a一端的电极是(填“正极”或“负极”),负极发生的电极反应是()。
 答案:
答案:
A.将所有的循环气体放散掉,再更换新的惰性气体
B.向循环气体喷洒化学试剂,便气体中的可燃成分发生化学反应,从而降低可燃成分浓度
C.连续放散部分循环气体,并相应地补充适当的惰性气体,从而降低可燃成分浓度
D.连续往升温后的循环气体中通入适量的空气燃烧掉增长的可燃成分,冷却后再放散掉相应的循环气体量,从而降低可燃成分浓度
工业上以氨气为原料制备硝酸的过程如下: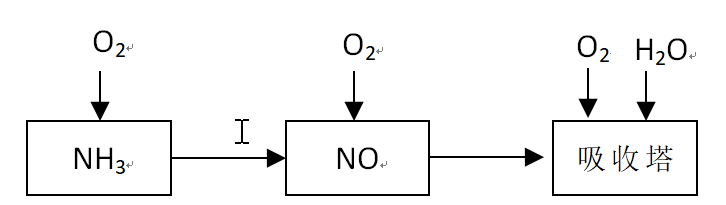 某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。
某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。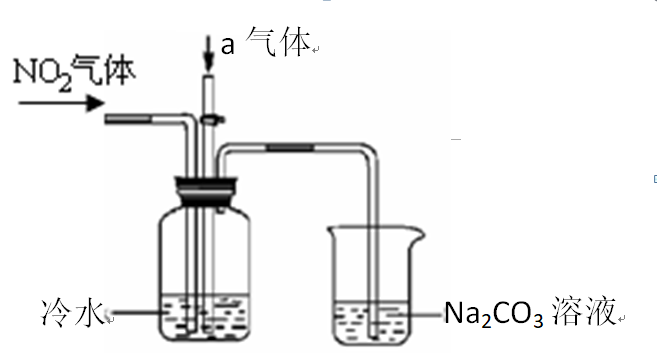
问题一、工业上用氨气制取NO的化学方程式是()。
问题二、连接好该装置后,首先进行的操作是()。
问题三、通入a气体的目的是()。
问题四、盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中反应的化学反应方程式是2NO2+Na2CO3==NaNO2+()+()
问题五、已知:温度低于21.15℃时,NO2几乎全部转变为N2O4.工业上可用N2O4与水反应来提高硝酸产率。N2O4与a气体在冷水中生成硝酸的化学方程式是()。
问题六、一定条件下,某密闭容器中N2O4和NO2的混合气体到达平衡时,c(NO2)=0.50mol/L、c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
A.水蒸馏法
B.冷压榨法
C.油脂分离法
D.溶剂萃取法