 更多“ICP工作原理是离子在高温下获得能量发生碰撞时,高能级电子跃…”相关的问题
更多“ICP工作原理是离子在高温下获得能量发生碰撞时,高能级电子跃…”相关的问题
第2题
某氮肥厂氨氮废水中的氮元素多以NH和NH3·H2O的形式存在,该废水的处理流程如下:![]()
问题一、过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。
①用离子方程式表示加NaOH溶液的作用:()。
②用化学平衡原理解释通空气的目的:()。
问题二、过程Ⅱ:在微生物作用的条件下,NH经过两步反应被氧化成NO。两步反应的能量变化示意图如下:
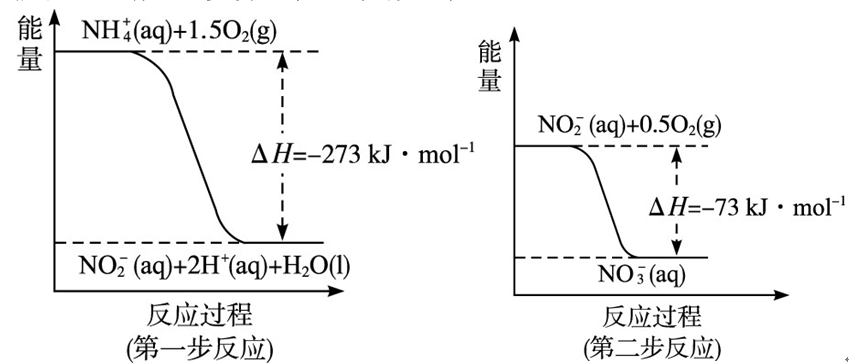
①第一步反应是()反应(选填“放热”或“吸热”),判断依据是()。
②1molNH(aq)全部氧化成NO(aq)的热化学方程式是()。
问题三、过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3复原成N2。假设该反应消耗32gCH3OH转移6mol电子,则参加反应的复原剂和氧化剂的物质的量之比是()。
第5题
感烟式火警探测器有两种,一种基于()原理,另一种基于()原理。
A.烟雾浓度不同透光程度不同/烟雾颗粒能吸收空气中被电离的离子
B.烟雾导电随浓度变化/烟雾颗粒在磁场中磁化
C.烟雾透光性/烟雾吸收α射线
D.烟雾顺磁性/烟雾逆磁性
第8题
非同一控制下的控股合并中,假如合并日被合并企业固定资产的公允价值高于其账面价值,在编制控制权获得后来首期合并财务报表时,对的的处理措施是()。
A.在账簿中将固定资产的账面价值调整为公允价值并增长资本公积
B.在账簿中将固定资产的账面价值调整为公允价值并增长营业外收入
C.在工作底稿中将固定资产的账面价值调整为公允价值并增长资本公积
D.在工作底稿中将固定资产的账面价值调整为公允价值并增长营业外收入


 如果结果不匹配,请
如果结果不匹配,请 
















