 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
写出下面电池的电极反应和电池反应,并计算298K时电池的电动势。已知电池的标准电动势为0.4402V。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“写出下面电池的电极反应和电池反应,并计算298K时电池的电动…”相关的问题
更多“写出下面电池的电极反应和电池反应,并计算298K时电池的电动…”相关的问题
写出下列各电池的电池反应。应用表7.7.1(在教材中)的数据计算25℃时各电池的电动势及电池反应的摩尔吉布斯函数变,并指明各电池反应能否自发进行。
(1)Pt|H2(g,100kPa)|HCl[a(HCl)=1]|Cl2(g,100kPa)|Pt
(2)Zn|ZnCl2[a(ZnCl2)=0.5]|AgCl(S)|Ag
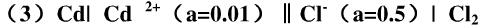
A.锂电极作电池负极,放电过程中发生还原反应
B.1 mol SOCl2发生电极反应转移的电子物质的量为4 mol
C.组装该电池必须在无水、无氧的条件下进行
D.电池的正极反应为2SOCl2+2e-=4Cl-+S+SO2 ↑
A.电极A上H2和CO都发生了氧化反应
B.反应CH4+H2O=3H2+CO,每消耗1 mol CH4转移12 mol电子
C.电池工作时,电能转变为化学能
D.电极B上发生的电极反应为:O2+2H2O+4e−=4OH−
最近科学家提出“绿色自由”设想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。“绿色自由”设想技术流程如下
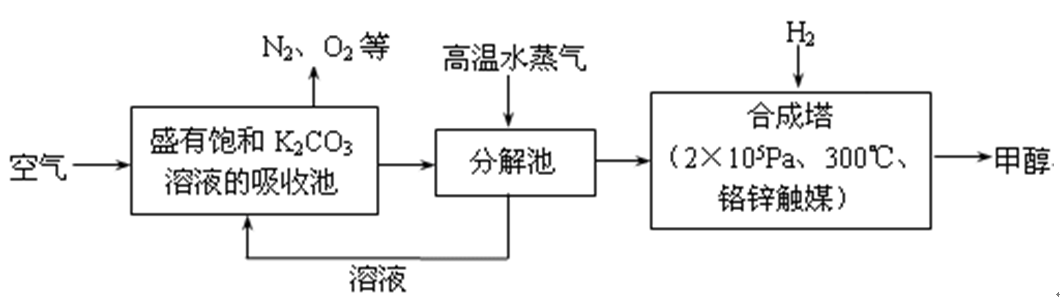
问题一、分解池中发生分解反应的物质是()。
问题二、在合成塔中,假设有CO2与足量H2kJ的热量,试写出合成塔中发生反应的热化学方程式()
问题三、①从平衡移动原理分析,低温有利于原料气的转化,而实际生产中采用300℃的温度,原因之一是考虑到催化剂的催化活性,原因之二是()。
②“绿色自由”设想技术流程中常包括物质和能量的“循环利用”,上述流程中能表达“循环利用”的除碳酸钾溶液外,还包括()。
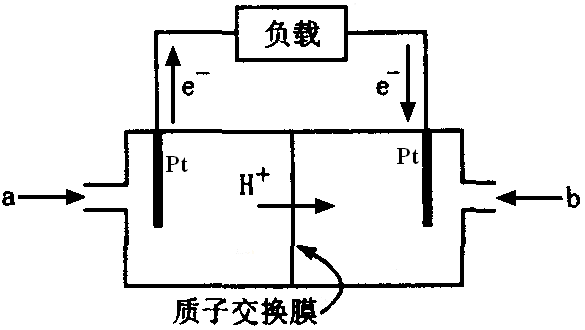
问题四、右图是甲醇燃料电池的结构示意图。已知电池总反应为:2CH3OH+3O2=2CO2+4H2O。通入a一端的电极是(填“正极”或“负极”),负极发生的电极反应是()。
 答案:
答案:
A.氢气在负极发生还原反应
B.供电时的总反应为:2H2+O2=2H2O
C.产物为无污染的水,属于环境友好电池
D.工作时电解质溶液的PH不断减少
A.放电时,Pb作为电池的负极发生还原反应
B.放电时,内电路中的H+ 向Pb电极移动
C.充电时,外接电源的负极需要与Pb电极相连
D.充电时,阳极区附近溶液酸性减弱
A.正极反应式为O2+2H2O+4e-=4OH-
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需更换铝板就可继续使用
A.正极的电极反应为O2+2H2O+2e﹣=4OH﹣
B.负极的电极反应为Al+3OH﹣﹣﹣3e﹣═AI(OH)3↓
C.电池工作过程中,电解液的pH保持不变
D.电池使用时可能析出H2并放热
A.氢气在负极发生氧化反应
B.供电时的总反应为:2H2+O2=H2O
C.正极:O2+4eˉ+2H2O=4OHˉ
D.电池在工作一段时间电解质溶液浓度不变
A.正极并被还原
B.正极并被氧化
C.负极并被还原
D.负极并被氧化
A.通CO的一极是电池的正极
B.负极发生的电极反应是O2+2CO2+4e-=2CO32-
C.负极发生的电极反应是CO+CO32--2e-=2CO2
D.正极发生氧化反应