 更多“清洗过程中Fe2+浓度为0.1mol/L,换算为mg/L表示…”相关的问题
更多“清洗过程中Fe2+浓度为0.1mol/L,换算为mg/L表示…”相关的问题
A.c(1/2Na2C03)=0.5mo1/L
B.c(Na2C03)=0.5mol/L
C.c(Na2C03)=1.Omo1/L
D.c(Na2C03)=0.1mol/L
A.0.02mo1/L
B.0.1mol/L
C.0.5mol/L
D.0.25mo1/L
以黄铁矿为原料制硫酸产生的废渣中含Fe2O3、SiO2、Al2O3、CaO、MgO等。现以此废渣制备铁红(Fe2O3)的过程如下。此浓度时,部分阳离子以氢氧化物形式沉淀时溶液的pH由见右表。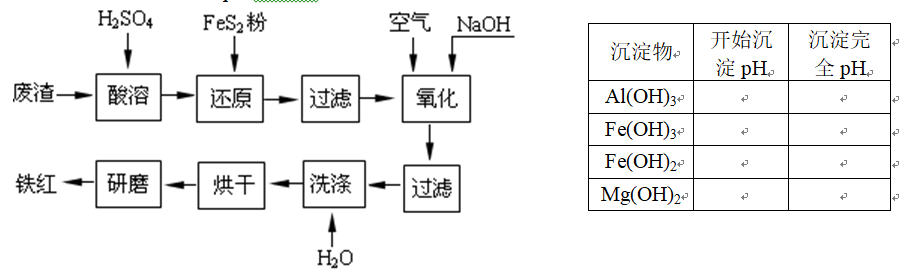 问题一、酸溶过程中Fe2O3与稀硫酸反应的化学方程式是()。
问题一、酸溶过程中Fe2O3与稀硫酸反应的化学方程式是()。
问题二、复原过程中加入FeS2是将溶液中的Fe3+复原为Fe2+,而本身被氧化为SO42-,写出有关的离子方程式:()。
问题三、氧化过程中通入空气和加入NaOH是为了将溶液中的铁元素充分转化为沉淀而析出,写出有关的离子方程式:()。
问题四、为了确保铁红的质量,氧化过程需要调节溶液pH的范围为()≤pH<()。
问题五、假设NaOH加入过量,所的铁红产品中有其它杂质,但可能无Al2O3,其原因是(用离子方程式表示):() 。
A.0.1mol/L的标准酸溶液定位
B.0.1mol/L的标准碱溶液定位
C.用pH为6.86的缓冲溶液定位
D.至少2个标准缓冲溶液定位
已知邻苯二甲酸氢钾(HKP用示表)的摩尔质量为204.2g/mol,用它来标定0.1mol/L的NaOH溶液,宜称取KHP质量为()。
A.0.25g左右
B.1g左右
C.0.6g左右
D.0.1g左右
随着工业的迅速发展,产生的废水对水体的污染也日趋严重。通过控制溶液的pH对工业废水中的金属离子进行别离是实际工作中经常使用的方法。下表是常温下金属氢氧化物的Ksp(沉淀溶解平衡常数)和金属离子在某浓度下开始沉淀所需的pH(表中浓度为相应pH时溶液中有关金属离子产生沉淀的最小浓度;当溶液中金属离子浓度小于10-5mol•L-1时通常认为该离子沉淀完全)。 问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题二、为了处理含有Cr2O72-酸性溶液的工业废水,采用如下方法:向废水中加人适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准
①Cr2O72-转变为Cr3+的离子方程式为()。
②pH对废水中Cr2072-去除率的影响如右图。你认为电解过程中溶液的pH取值在()范围内对降低废水中的铬含量最有利,请说明理由:()。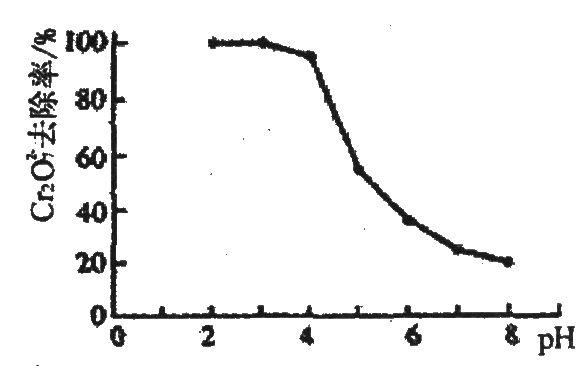
问题三、沉淀转化在生产中也有重要应用。例如,用Na2C03溶液可以将锅炉水垢中的CaS04转化为较疏松而易清除的CaC03,该沉淀转化到达平衡时,其平衡常数K=()。(已知Ksp(CaS04)=9.1x10-6,Ksp(CaC03)=2.8x10-9)


 如果结果不匹配,请
如果结果不匹配,请 
















