 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知Eθ(Ag+/Ag)=0.799 1 V,在电极的溶液中加入K2 CrO4(s)(忽略体积变化),达平衡后c(CrO42-)=0.50
已知Eθ(Ag+/Ag)=0.799 1 V,在电极的溶液中加入K2 CrO4(s)(忽略体积变化),达平衡后c(CrO42-)=0.500 mol.dm-3,Ksp(Ag2CrO4)=1.2×10-12,则新电极反应的标准电势值与下列数据中最接近的是 ()
A.1.603 V
B.0.401 V
C.0.622 V
D.0.433 V
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“已知Eθ(Ag+/Ag)=0.799 1 V,在电极的溶液中…”相关的问题
更多“已知Eθ(Ag+/Ag)=0.799 1 V,在电极的溶液中…”相关的问题
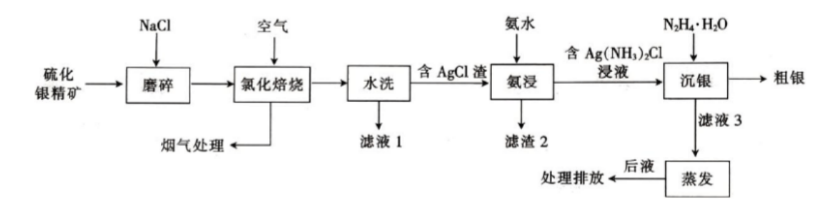 已知:氯化焙烧时,氧化物不参与反应,硫化物转化为氯化物;氯化铅不溶于水,溶于氯化钠溶液。
已知:氯化焙烧时,氧化物不参与反应,硫化物转化为氯化物;氯化铅不溶于水,溶于氯化钠溶液。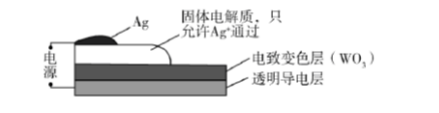

 。
。















