 更多“所有的盐在水溶液中都发生水解()”相关的问题
更多“所有的盐在水溶液中都发生水解()”相关的问题
A.分子中含巯基,水溶液易发生氧化反应
B.分子中含联苯和四唑结构
C.分子中有两个手性碳,顺式d-异构体对冠脉扩张作用强而持久
D.结构中含单乙酯,为一前药
E.为一种前药,在体内,内酯环水解为β-羟基酸衍生物才具活性
聚合氯化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝(Al2(OH)nCl6-n)。本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下
 根据流程图答复以下问题:
根据流程图答复以下问题:
问题一、“煅烧”的目的是()。
问题二、配制质量分数15%的盐酸需要200mL30%的浓盐酸(密度约为1.15g·cm-3)和()g蒸馏水,配制用到的仪器有烧杯、玻璃棒、()。
问题三、“溶解”过程中发生反应的离子方程式为()。
问题四、加少量铝粉的主要作用是()。
问题五、“调节溶液pH在~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是();“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是()。
有关汞的处理错误的选项是()。
A.汞盐废液先调节pH值至8~10,参加过量Na2S后再参加FeSO4生成HgS、FeS共沉淀再作回收处理
B.洒落在地上的汞可用硫黄粉盖上,干后清扫
C.实验台上的汞可采用适当措施收集在有水的烧杯
D.散落过汞的地面可喷洒20%FeCl2水溶液,干后清扫
高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O Na2FeO4+2KOH=K2FeO4+2NaOH 主要的生产流程如下: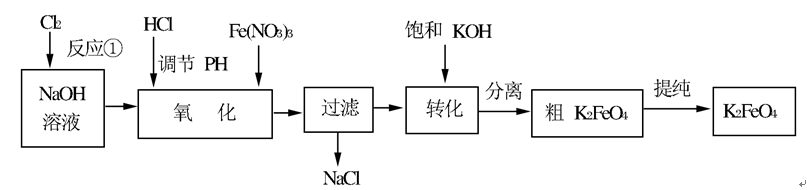 问题一、写出反应①的离子方程式()。
问题一、写出反应①的离子方程式()。
问题二、流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4)()Ksp(Na2FeO4)〔填“>”或“<”或“=”〕。
问题三、反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。
图1为不同的温度下,Fe(NO3)3不同质量浓度对生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最正确时,NaClO浓度对K2FeO4生成率的影响
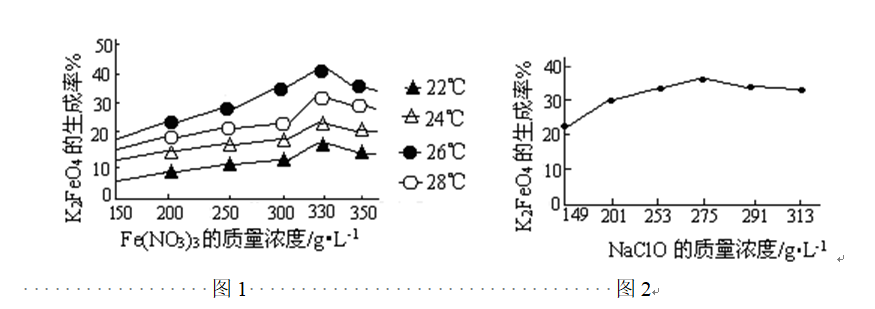
①工业生产中最正确温度为()℃,此时Fe(NO3)3与NaClO两种溶液最正确质量浓度之比为()。
②假设NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:()。假设Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化复原反应生成K3FeO4,此反应的离子方程式:()。
问题四、K2FeO4在水溶液中易水解:
4FeO42—+10H2O 4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
AH2O
BCH3COONa、异丙醇
CNH4Cl、异丙醇
DFe(NO3)3、异丙醇


 如果结果不匹配,请
如果结果不匹配,请 
















