 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将锌片浸入含有0.01mol/L浓度的 溶液中,已知 =-0.762V,则25°C时,锌电极的电极电势为()
A.-0.762V
B.-0.801V
C.-0.821V
D.-0.703V
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.-0.762V
B.-0.801V
C.-0.821V
D.-0.703V
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“将锌片浸入含有0.01mol/L浓度的 溶液中,已知 =-0…”相关的问题
更多“将锌片浸入含有0.01mol/L浓度的 溶液中,已知 =-0…”相关的问题
A.可能含有Na+
B.可能含有SO42-
C.一定不含Cl-
D.一定含有NH4+
A.甲容器中电子由锌片流向铜片
B.两烧杯溶液中的硫酸浓度均减少
C.甲中铜片是正极,乙中铜片是负极
D.甲容器中溶液即使换成酒精也可以形成原电池
A.铁片产生气体速率快,说明铁比锌活泼
B.锌片产生气体速率快,说明锌比铁活泼
C.铁片产生气体速率慢,说明铁比锌活泼
D.锌片产生气体速率慢,说明锌比铁活泼
A.0.01mol
B.0.02 mol
C.0.03 mol
D.0.04 mol
A.HY一定是弱酸
B.酸性HX>HY
C.HX一定是强酸
D.反应开始时二者生成H2的速率相同
A.300mg/L,5分钟
B.250mg/L,5分钟
C.300mg/L,10分钟
D.250mg/L,10分钟
苯乙烯在60℃以过氧化二叔丁基为引发剂,苯为溶剂进行溶液聚合。当单体苯乙烯的浓度c(M)=1mol/L,引发剂浓度c(I)=0.01mol/L时,引发和聚合的初速分别为4×10-11mol/(L·s)和1.5×10-7mol/(L·s)。试根据计算判断低转化率下,在上述聚合反应中链终止的主要方式,真正终止和链转移终止的比例。已知:60℃时CM=8.0×10-5,CI=3.2×10-4,CS=2.3×10-6,苯乙烯的密度为0.887g/mL,苯的密度为0.839g/mL。设苯乙烯苯体系为理想溶液。
末期反应时间与转化率
蔗糖在稀水溶液中水解生成葡萄糖和果糖的反应为
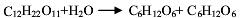

当水大大过量时,反应遵循一级反应动力学,即(-rA)=kcA,在催化剂HCl浓度为0.01mol/L,反应温度为48℃时,反应速率常数为k=0.0193min-1。当蔗糖的浓度为0.1mol/L和0.5mol/L时计算:
(1)反应20min后,上述两种初始浓度下反应液中蔗糖、葡萄糖和果糖的浓度分别为多少?
(2)试计算两种初始浓度的溶液中蔗糖的转化率各为多少?
(3)若蔗糖浓度降到0.01min/L时,两种初始浓度条件下所需反应时间各为多少?
A.10min内,X的平均反应速率为0.01mol/(L·min)
B.第10min时,X的反应速率为0.01mol/(L·min)
C.10min内,消耗0.1mol X,生成0.4mol Z
D.10min内,X和Y反应放出的热量为92kJ