 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列说法正确的是()
A.用甲装置电解精炼镁
B.用乙装置试管中有氨气生成
C.用丙装置构成铜锌原电池
D.用丁装置对二次电池进行充电
 答案
答案
C、用丙装置构成铜锌原电池
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.用甲装置电解精炼镁
B.用乙装置试管中有氨气生成
C.用丙装置构成铜锌原电池
D.用丁装置对二次电池进行充电
 答案
答案
C、用丙装置构成铜锌原电池
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列说法正确的是()”相关的问题
更多“下列说法正确的是()”相关的问题
电解工作原理的实际应用非常广泛。
(1)请画出铜棒镀银的简易装置设计图()。(实验可选用品:铜棒,银片,石墨棒,硫酸铜溶液,硝酸银溶液,导线,电源,烧杯)。
(2)工业上为了处理含有Cr2O12-的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是()(填字母)。
A、阳极反应:Fe-2e-=Fe2+
B、阴极反应:2H++2e-=H2↑
C、在电解过程中工业废水由酸性变为碱性
D、可以将铁电极改为石墨电极
(3)某同学设计了如图装置进行以下电化学实验。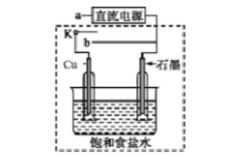 ①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。
①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为()。请写出此时Cu电极上的电极反应()。
(4)某溶液中含有的离子如下表: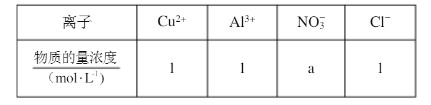 用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。
用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。
A、电解后溶液呈酸性
B、a=3
C、阳极生成1.5molCl2
D、阴极析出的金属是铜与铝
A.甲成立非法携带危险物品危及公共安全罪
B.甲对爆炸结果的发生是一种过失
C.甲成立过失致人死亡罪
D.对甲应当以爆炸罪和非法携带危险物品危及公共安全罪数罪并罚
A.在浓酸储存处应设置防泄漏设施
B.电解液循环系统应设置酸雾排空装置
C.操作人员离烫洗槽应保持0.1m以上
D.电解液存放设施需设置应急泵
A.脱砷应设抽风系统
B.应设置砷化合物自动检测报警器
C.脱砷岗位等区域应设置冲淋、洗眼装置
D.电积脱砷槽出装槽前须停电5min以上。并保持抽风
A.①泡抗菌液5分种→②红外线理疗灯照至80%干→③用产品护理指甲和皮肤
B.浸泡杀菌核心产品皮肤抗菌液、抗菌液、Ⅱ代抗菌液。总体杀菌时间不得低于28天
C.指甲护理滴涂产品顺序:①凤仙花抑菌液或②抗菌液(高浓缩)+涂精蒜素
D.整个手、足皮肤护理涂绿软膏和①凤仙花抗菌膏或②抗菌膏
芒硝化学式为Na2SO4·10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。用如图所示装置电解硫酸钠溶液,模拟工业上离子交换膜法制烧碱的方法。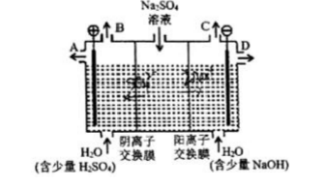 (1)该电解槽的阴极反应式为()。
(1)该电解槽的阴极反应式为()。
(2)电解时,通过阴离子交换膜的离子数()通过阳离子交换膜的离子数。(填大于、小于或等于)。
(3)制得的氢氧化钠溶液从出口()(填写“A”、“B”、“C”、“D”)导出。
(4)①若将制得的氧气、氢氧化钠溶液与天然气组合为甲烷燃料电池,则电池负极的电极反应式为()。
②若将该电池连接两惰性电极,用于电解800mLlmol/L的AgNO3溶液,当原电池中消耗CH4的体积在标况下为0.224L时,电解池中阴极将得到()g的单质,电解池中H+的浓度为()(假设溶液体积不变)。
A.W总甲> W总乙>W总丙
B.W总甲< W总乙<W总丙
C.W总甲=W总乙=W总丙
D.无法判断