 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在427℃时各物质的热力学函数 在该温度下反应N2+3H2(g)====2NH3(g)达平衡时,[N2]=1.0mol·dm-3,[
已知在427℃时各物质的热力学函数
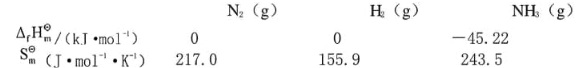 在该温度下反应N2+3H2(g)====2NH3(g)达平衡时,[N2]=1.0mol·dm-3,[H2]=3.0mol·dm-3。求NH3的浓度。
在该温度下反应N2+3H2(g)====2NH3(g)达平衡时,[N2]=1.0mol·dm-3,[H2]=3.0mol·dm-3。求NH3的浓度。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在427℃时各物质的热力学函数
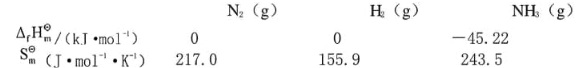 在该温度下反应N2+3H2(g)====2NH3(g)达平衡时,[N2]=1.0mol·dm-3,[H2]=3.0mol·dm-3。求NH3的浓度。
在该温度下反应N2+3H2(g)====2NH3(g)达平衡时,[N2]=1.0mol·dm-3,[H2]=3.0mol·dm-3。求NH3的浓度。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知在427℃时各物质的热力学函数 在该温度下反应N2+3H…”相关的问题
更多“已知在427℃时各物质的热力学函数 在该温度下反应N2+3H…”相关的问题
A.纯理想气体的标准状态就是标准压力P(100KPa)下的状态
B.纯液体物质的标准状态就是标准压力P(100KPa)下的纯液体
C.纯固体物质的标准状态就是标准压力P(100KPa)下的纯固体
D.不同的物质在相同温度下都处于标准状态时,它们的同一热力学函数值都应相同
A.X2为0.2
B.Y2为0.2
C.Z为0.3
D.Z为0
在298K时,下述电池的电动势E=0.1519V:
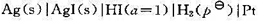
并已知下列物质的标准摩尔生成焓:
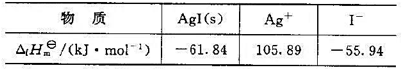
试求:(1)当电池可逆输出1mol电子的电荷量时,Q.W.(膨胀功)、W:(电功)和电池反应的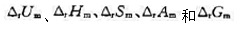 、 和 的值各为多少;(2)如果让电池短路,不做电功,则在发生同样的反应时上述各函数的变量又为多少。
、 和 的值各为多少;(2)如果让电池短路,不做电功,则在发生同样的反应时上述各函数的变量又为多少。
对于化学反应:CH4(g)+H2O(g)===CO(g)+3H2(g),应用附录(在教材中)中各物质在25℃时的标准摩尔生成焓数据及摩尔定压热容与温度的函数关系式:(1)表示成温度的函数关系式;(2)求该反应在1000K下的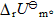 。
。
在298K和101 325Pa条件下,配制1000cm3的甲醇(B)水(A)溶液,溶液浓度为xB=0.3。已知该浓度时偏摩尔体积VB,m=38.632ml/mol,vA,m=17.765ml/mol,纯态时摩尔体积VB=40.772ml/mol,VA=18.062ml/mol。 (1)需要纯水和纯甲醇各多少? (2)混合过程体积变化多少?
A.物质的量浓度相同时,各溶液的pH关系为pH(Na2Y)>pH(NaX)>pH(NaHY)
B.mol·L-1HX溶液与bmol·L-1NaOH溶液等体积混合,所得溶液中存在c(Na+)>c(X-),则不一定a<b
C.在HX溶液中滴入Na2Y溶液,反应2HX+Y2-===2X-+H2Y成立
D.若0.1mol·L-1NaHY溶液呈酸性,则其水解能力小于电离能力