 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
于某药物的 Na 2 CO 3 溶液中滴加 AgNO 3 试液, 开始生成白色沉淀, 经振摇即溶解, 继续滴加 AgNO 3试液, 生成的白色沉淀经振摇则不再溶解,该药物应就是()
A.盐酸普鲁卡因
B.异戊巴比妥
C.地西泮
D.咖啡因
E.四环素
 答案
答案
B、异戊巴比妥
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.盐酸普鲁卡因
B.异戊巴比妥
C.地西泮
D.咖啡因
E.四环素
 答案
答案
B、异戊巴比妥
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“于某药物的 Na 2 CO 3 溶液中滴加 AgNO 3 试…”相关的问题
更多“于某药物的 Na 2 CO 3 溶液中滴加 AgNO 3 试…”相关的问题
A.由步骤(1)可知,白色粉末中一定含碳酸钠和氢氧化钙
B.步骤(2)结束后所得溶液中溶质除酚酞外,只有氯化钠和氢氧化钠
C.该白色粉末的组成一定是碳酸钠、氢氧化钙和碳酸钙
D.该白色粉末中一定含碳酸钙
A.由步骤(1)可知,白色粉末中一定含碳酸钠和氢氧化钙
B.步骤(2)结束后所得溶液中溶质除酚酞外,只有氯化钠和氢氧化钠
C.该白色粉末的组成可能是碳酸钠、氢氧化钙和碳酸钙
D.该白色粉末中可能含碳酸钙
A.样品中一定含有KNO₃
B.样品中一定含有Na₂CO₃
C.样品中可能含有Ba(NO₃)₂
D.样品中可能含有Na₂CO₃和KNO₃
A.切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2=Na2O2
B.向AgC1悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2-=Ag2S↓+2Cl-
C.Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物:2Na2O2+CO2=2Na2CO3+O2
D.FeCl2溶液中滴加NaClO溶液生成红褐色沉淀:2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+
A.密闭容器中2 mol NO与1 mol O2充分反应,产物分子的数目为2NA
B.25℃,pH=13的NaOH溶液中含有OH-的数目为 0.1NA
C.标准状况下,22.4 L CCl4含CCl4分子数为NA
D.标准状况下,22.4L N2与CO混合气体的质量为28g
A.CO2通入NaAlO2溶液中AlO+CO2+H2O===Al(OH)3↓+CO
B.Al2O3与过量氨水Al2O3+6NH3•H2O===2Al3++6NH
C.向AlCl3溶液中加入过量NaOH溶液Al3++3OH-===Al(OH)3↓
D.向AlCl3溶液中滴入过量的氨水Al3++3NH3•H2O===Al(OH)3↓+3NH
A.向某溶液中加入2滴KSCN溶液,溶液不显血红色,再向溶液中加入几滴新制的氯水,溶液变为血红色,该溶液中一定含Fe2+
B.为检验红砖中铁的价态,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴,溶液变为血红色,说明红砖中只有三氧化二铁
C.N溶液,出现血红色,说明检验前该试样已变质
D.制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁
E.将(NH4)2Fe(SO4)2•6H2O试样溶于稀硝酸中,滴加KS
A.名称 白醋 稀盐酸 氯化钠
B.溶液 蒸馏水 石灰水 氢氧化
C.钾溶液 X汁液 红色 红色 紫色 紫色 绿色 绿色 (1)据上表推测,X汁液 (填能或不能)作酸碱指示剂
D.(2)将X汁液滴入肥皂水中溶液呈绿色,则 (填酸碱或中)性,pH (填><或=)7
E.(3)粗略测定雨水的酸碱度可使用
A.Na₂CO₃固体(NaHCO₃)—充分加热至固体质量不再改变
B.u(Fe)—加过量稀盐酸后过滤、洗涤、干燥
C.NaOH溶液(Na₂CO₃)—加入适量氢氧化钙溶液,过滤
D.O₂(HCl)—通过盛氢氧化钠
A.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
B.78 g苯含有C= C双键的数目为3 NA
C.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA
D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1 NA
K3[Fe(C2O4)3]•3H2O(三草酸合铁酸钾)为亮绿色晶体,易溶于水,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室用莫尔盐[(NH4)2Fe(SO4)2•6H2O]制备K3[Fe(C2O4)3]•3H2O的流程如图1所示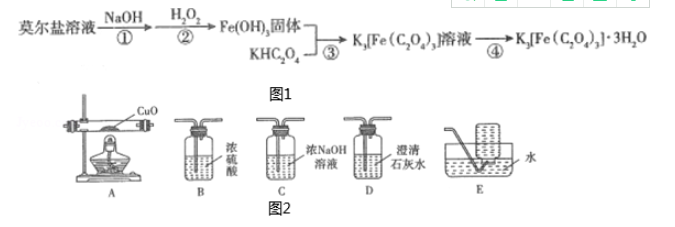 。回答下列问题:
。回答下列问题:
问题1、K3[Fe(C2O4)3]中铁离子的配位数为,其配体C2O42﹣中C原子的杂化方式为()。
问题2、步骤②发生反应的化学方程式为()。
问题3、步骤③将Fe(OH)3加入到KHC2O4溶液中,水浴加热,控制溶液pH为3.0~3.5,随反应进行需加入适量()。(已知:常温下KHC2O4溶液的pH约为3.5)
问题4、得到的三草酸合铁酸钾晶体依次用少量冰水、95%乙醇洗涤的目的是()。
问题5、某研究小组将K3[Fe(C2O4)3]•3H2O在一定条件下加热分解,利用图2装置(可重复使用)验证所得气体产物中含有CO和CO2。 ①按气流从左到右的方向,依次连接的合理顺序为()。(填装置序号) ②确认气体产物中含CO的现象()。