 更多“在Mn的还原过程中,是其还原的首要条件是一个重要条件。”相关的问题
更多“在Mn的还原过程中,是其还原的首要条件是一个重要条件。”相关的问题
第5题
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3 。则下列说法错误的是()
A.反应过程中,被氧化与被还原的元素的物质的量之比为1:2
B.NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉
C.若反应中转移的电子数目为6.02×1023,则可生成22.4L NO气体(标准状况)
D.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染
第6题
KMnO4是一种重要消毒剂,俗名叫灰锰氧。
Ⅰ.某工厂以废旧锌锰电池为原料制备高锰酸钾的流程如下(部分产物已省略)
回答下列问题: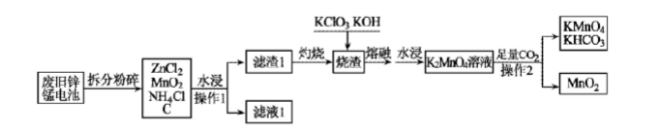 (1)K+的结构示意图为()。
(1)K+的结构示意图为()。
(2)这种锌锰电池放电时,负极的电极反应式为()。
(3)滤渣1“灼烧”的目的是();可循环利用的物质是()(填化学式)。
(4)“水浸”采用适当加热搅拌等措施,其目的是(),熔融“烧渣”可能产生的大气污染物是()。
(5)向K2MnO4溶液中通入足量CO2的离子方程式为:()。
Ⅱ.实验室中利用K2MnO4进行如下实验,下列说法错误的是()。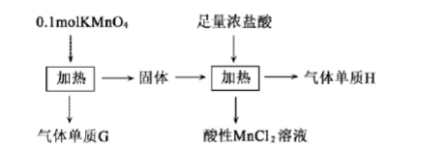 A、G与H均为氧化产物
A、G与H均为氧化产物
B、实验中KMnO4只作氧化剂
C、Mn元素至少参与了3个氧化还原反应
D、G与H的物质的量之和可能为0.25mol
第9题
某一产品的生产过程包括硝化、还原、置换三个步骤,各步的操作周期分别为24h、8h12h、,全部物料均为液体,且在整个生产过程中的体积保持不变若要保持各设备之间的能力平衡,则下列几种安排中不合理的是()。
A.1000L硝化釜3只,500L还原釜2只,1500L置换釜1只
B.1500L硝化釜2只,500L还原釜2只,500置换釜3只
C.1500L硝化釜2只,500L还原釜3只,1500置换釜2只
D.3000L硝化釜1只,1000L还原釜1只,1500置换釜1只
第11题
对炉渣性能的要求是()。
A.有良好的流动性,不给冶炼操作带来任何困难
B.有参与所希望的化学反应的充分能力,如(Si)、(Mn)或其它有益元素的还原,吸收S及碱金属等
C.能满足允许煤气顺利通过及渣铁,渣气良好分离的力学条件
D.稳定性好,即不致因冶炼条件的改变炉渣性能急剧恶化


 如果结果不匹配,请
如果结果不匹配,请 
















