 更多“根据电势图计算在298K时,Br2在碱性水溶液中歧化为Br¯”相关的问题
更多“根据电势图计算在298K时,Br2在碱性水溶液中歧化为Br¯”相关的问题
根据下列反应(假设离子浓度均为1.0molL-1) Ni(s)+Sn2+(aq)=Ni2+(aq)+Sn(s) Cl2(g)+2Br-1(aq)=Br2(l)+2Cl-(aq) 试分别计算: (1)它们组成的原电池电动势,并指出正负极。 (2)298K时的平衡常数。 (3)298K反应的标准吉布斯函数变△rGΘm。
根据PbI2的溶度积常数,计算在25℃ 时的下列参数: (1)PbI2在水中的溶解度; (2)在PbI2饱和溶
根据PbI2的溶度积常数,计算在25℃ 时的下列参数: (1)PbI2在水中的溶解度; (2)在PbI2饱和溶液中Pb2+离子和I-离子的浓度; (3)PbI2在浓度为0.010 mol.dm-3的KI溶液中达到饱和时,溶液中的Pb2+离子浓度; (4)PbI2在浓度为0.010 mol.dm-3的Pb(NO3)2溶液中的溶解度。
在298K和标准压力下,以Pt为阴极,C(石墨)为阳极,电解含CdCl2(0.01mol·kg-1)和CuCl2(0.02mol·kg-1)的水溶液。若电解过程中超电势可忽略不计, (设活度因子均为1),试问:
(设活度因子均为1),试问:

CO(CH2COOH)2在水溶液中分解成丙酮和二氧化碳,分解反应的速率 常数在283K时为1.08×10-4mol·L-1·s-1,在333K时为5.48×10-2mol·L-1·s-1,试计算在303K时分解反应的速率常数。
在不加催化剂时,H2O2的分解反应
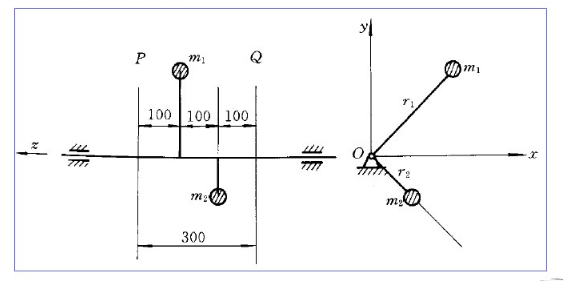
图(a)所示为一回转体,其上有不平衡质量m1=1kg,m2=2kg,与转动轴线的距离分别为r1=300mm,r2=150mm,m2r2与x轴正向的夹角分别为45°和315°。试计算在P,Q两平衡校正面上应加的平衡质径积(mbrb)p和(mbrb)Q的大小和方位。
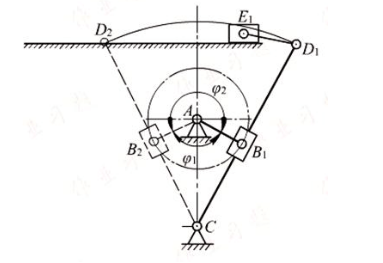
在图所示的刨床机构中,已知空程和工作行程中消耗于克服阻抗力的恒功率分别为P1=367.7W和P2=3677W,曲柄的平均转速n=100r/min,空程曲柄的转角为φ=120°。当机构的运转不均匀系数δ=0.05时,试确定电动机所需的平均功率,并分别计算在以下两种情况中的飞轮转动惯量JF(略去各构件的重量和转动惯量):
(1)飞轮装在曲柄轴上;
(2)飞轮装在电动机轴上,电动机的额定转速nn=1440r/min。电动机通过减速器驱动曲柄,为简化计算,减速器的转动惯量忽略不计。
A.确定导线的型号及设计气象区,确定导线在各种气象条件时的比载
B.确定导线的安全系数及防振措施
C.计算导线最大使用应力和年平均运行应力
D.计算临界档距并进行有效临界档距判别
E.计算在各种气象条件下各种代表档距值时的应力和弧垂值,绘制各种气象条件时的应力、弧垂曲线


 如果结果不匹配,请
如果结果不匹配,请 

















