题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电池Zn|ZnCl2(0.05mol·kg1)|AgCl(s)|Ag(s)的电动势与温度的关系为EV=1.0154.92×104(RK298)。试计算在2
电池Zn|ZnCl2(0.05mol·kg-1)|AgCl(s)|Ag(s)的电动势与温度的关系为E/V=1.015-4.92×10-4(R/K-298)。试计算在298K,当电池有2mol电子的电荷量输出时,电池反应的△rGm、△rHm、△rSm和此过程的可逆热效应QR。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“电池Zn|ZnCl2(0.05mol·kg1)|AgCl(s…”相关的问题
更多“电池Zn|ZnCl2(0.05mol·kg1)|AgCl(s…”相关的问题
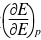 为-4.92×10-4V/K,试写出电池反应并计算当电池有2mol电子电量输出时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。
为-4.92×10-4V/K,试写出电池反应并计算当电池有2mol电子电量输出时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。