 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列有关工业炼铁的说法正确的是()
A.工业炼铁的主要设备是高炉
B.炼得的铁是银白色的纯净物
C.工业炼铁产生的废气对空气无害,可以直接排放
D.黄铁矿(主要成分FeS2)比赤铁矿(主要成分Fe2O3)更适合炼铁
 答案
答案
A、工业炼铁的主要设备是高炉
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.工业炼铁的主要设备是高炉
B.炼得的铁是银白色的纯净物
C.工业炼铁产生的废气对空气无害,可以直接排放
D.黄铁矿(主要成分FeS2)比赤铁矿(主要成分Fe2O3)更适合炼铁
 答案
答案
A、工业炼铁的主要设备是高炉
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列有关工业炼铁的说法正确的是()”相关的问题
更多“下列有关工业炼铁的说法正确的是()”相关的问题
A.《物理小识》中记载的是以焦炭作为还原剂的方法来炼铁
B.文中说明以煤炭作为燃料被普遍使用,煤的主要成分为烃
C.生铁是指含硫、磷、碳量低的铁合金
D.工业上可通过煤的干馏获得乙烯、丙烯等化工原料
如图为实验室模拟还原氧化铁的实验装置(夹持仪器等省略),已知: 。下列说法合理的是()。
。下列说法合理的是()。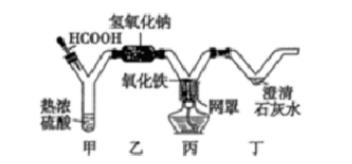
A.
装置丙中发生反应的化学方程式为:
B.装置乙中氢氧化钠的作用是吸收、除去二氧化碳
C.与课本模拟工业炼铁装置相比,该装置环保无污染
D.装置丁处装入澄清石灰水的目的是检验生成的CO2
A.酸雨形成的原因:CO2+H2O=== H2CO3
B.工业上用赤铁矿炼铁
C.证明铜的活动性强于银:Cu+2AgCl=== 2Ag+CuCl2
D.用含氢氧化铝的药物治疗胃酸过多:Al(OH)3+3HCl=== AlCl3+3H2O
A.酸雨形成的原因:CO2+H2O===== H2CO3 化合反应
B.工业上用赤铁矿炼铁:Fe3O4+4CO=====(高温)3Fe+4CO2 还原反应
C.证明铜的活动性强于银:Cu+2AgCl=====2Ag+CuCl2 置换反应
D.用含氢氧化铝的药物治疗胃酸过多:Al(OH)3+3HCl===== AlCl3+3H2O 复分解反应
A.使用的设备是高炉
B.主要原料为铁矿石、石灰石、焦炭和热空气等
C.主要原理是:2Fe2O3+3C===4Fe+3CO2↑
D.主要产物为生铁
A.磁铁矿的主要成分是Fe2O3
B.应先加热Fe2O3,再通入CO
C.红棕色的Fe2O3逐渐变黑
D.气体通过澄清石灰水后可直接排放
A.升高温度,反应速率减慢
B.当反应达到化学平衡时,υ(正)=υ(逆)=0
C.提高炼铁高炉的高度可减少尾气中CO的浓度
D.某温度下达到平衡时CO的体积分数基本不变