 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K,1molO2从101.325Pa绝热可逆压缩到6×101325Pa,求Q、W、ΔU、ΔH、ΔG、ΔS。已知298K氧的规定熵为205.03J/(K·mol)
298K,1molO2从101.325Pa绝热可逆压缩到6×101325Pa,求Q、W、ΔU、ΔH、ΔG、ΔS。已知298K氧的规定熵为205.03J/(K·mol)。(氧为双原子分子,若为理想气体,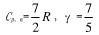 )
)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K,1molO2从101.325Pa绝热可逆压缩到6×101325Pa,求Q、W、ΔU、ΔH、ΔG、ΔS。已知298K氧的规定熵为205.03J/(K·mol)。(氧为双原子分子,若为理想气体,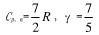 )
)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298K,1molO2从101.325Pa绝热可逆压缩到6×…”相关的问题
更多“298K,1molO2从101.325Pa绝热可逆压缩到6×…”相关的问题
有5mol He(g),可看做理想气体,已知其CV,m=1.5R,从始态273K、100kPa变到终态298K、1000kPa,求该过程的熵变。
A.足量MnO2和100mL6mol/L浓盐酸反应产生Cl2的分子数为0.15NA
B.100mL1molFeCl3溶液中所含Fe3+的数目为0.1NA
C.48g正丁烷和10g异丁烷的混合物中碳碳单键的数目为3NA
D.密闭容器中,2molSO2和1molO2催化反应后分子总数为2NA
A.容器中三氧化硫体积保持不变
B.容器中混合物的压强保持不变
C.混合物的总的物质的量保持不变
D.容器中SO2、O2与SO3的物质的量之比为2︰1︰2
A.容器中,SO2、O2与SO3共存且浓度相等
B.容器中,SO2、O2与SO3的物质的量之比为2︰1︰2
C.正反应生成SO3的速率等于逆反应生成O2的速率
D.反应容器内混合气体平均相对分子质量不随时间的变化而改变
A.容器内压强不再变化,说明反应达到平衡状态
B.当c(SO2):c(O2)=2:1表明反应达到平衡状态
C.加入合适的催化剂可显著增大反应速率,提高SO2的转化率
D.达到平衡状态时,相同时间内,每消耗2molSO3的同时生成1molO2
A.容器中,SO2、O2与SO3共存且浓度相等
B.容器中,SO2、O2与SO3的物质的量之比为2︰1︰2
C.正反应生成SO3的速率等于逆反应生成O2的速率
D.反应容器内混合气体平均式量不随时间的变化而改变
①2NH₃(g)→N₂(g)+3H₂(g)rHmΘ=92.2kJ·mol—1
②H₂(g)+ 1/2O₂(g)→H₂O(g)rHmΘ=-241.8 kJ·mol-1
③4NH₃(g)+5O₂(g)→4NO(g)+6H₂O(g)rHmΘ=-905。6 kJ·mol-1
试确定fHmΘ(NH₃,g,298K)=()kJ·mol-1;fHmΘ(H₂O,g,298K)=()kJ·mol—1;fHmΘ(NO,g,298K)=()kJ·mol—1。由NH₃(g)生产1.00kgNO(g)则放出热量为()kJ。
反应N2O5→2NO2+1/2O2在298K时的速率常数为3.46×10-5s-1,在318K时的速率常数为4.98×10-4s-1,则308K时的反应速率常数为()10-4s-1。(保留两位小数)